Эффективность препарата при инфекционном перитоните кошек, доказанная в официально зарегистрированных мультицентровых рандомизированных клинических и постклинических исследованиях.
Сведения об авторах:
Аффилиации:
- Ветеринарная клиника «Триовет» (105094, РФ, г. Москва, Госпитальный Вал, д. 3, кор. 5).
- Компания ООО «Ветстем» (121205, РФ, г. Москва, территория Сколково инновационного центра, Большой бульвар, д. 42, стр. 1).
Параметры исследования:
- Период: июнь 2023 - апрель 2024.
- 28 кошек, в возрасте от 6 месяцев до 11 лет.
- 18 животных с экссудативной и 10 с неэкссудативной формой ИПК/FIP.
- 3 группы с учетом стартовой разовой дозы препарата Ипекон®: 8 мг/кг, 10 мг/кг, 12 мг/кг.
Ключевые слова:
- Инфекционный перитонит кошек
- ИПК
- FIP
- Кошачий коронавирус
- Ипекон®
- Вефинавир
- VS-121354
- Ингибитор вирусной протеазы
Аннотация
Инфекционный перитонит кошек — трудноизлечимое заболевание, вызываемое высоковирулентным биотипом широко распространенного кошачьего коронавируса. Компания ООО «Ветстем» разработала лекарственный препарат Ипекон® на основе низкомолекулярного соединения с прямым противовирусным эффектом в отношении РНК-содержащих вирусов. Ипекон® прошел все доклинические исследования.
Цель исследования
Оценить терапевтическую эффективность лекарственного препарата для ветеринарного применения Ипекон® при лечении инфекционного перитонита кошек.
Материалы и методы
В исследование включили 28 кошек, в возрасте от 6 месяцев до 11 лет: 18 животных с экссудативной и 10 с неэкссудативной («сухой») формой ИПК/FIP. Животные были распределены на 3 группы с учетом стартовой разовой дозы препарата Ипекон®: 8 мг/кг, 10 мг/кг, 12 мг/кг. Готовый раствор вводили подкожно ежедневно, один раз в день, с интервалом между инъекциями 24 ч в течение всего курса лечения. Оценка эффективности лечения была комплексной, с учетом данных клинического осмотра, результатов общеклинического и биохимического анализов крови, УЗИ внутренних органов.
Результаты
Из 28 животных с диагностированным ИПК/FIP, включенных в исследование, у 4 (14,3 %) пациентов зафиксирован летальный исход, вызванный полиорганной недостаточностью; 85,7 % пациентов по окончании курсового лечения имели статус «клиническое выздоровление». Установлена хорошая переносимость препарата Ипекон® при многократном подкожном применении. Несмотря на отмеченный дискомфорт при введении, признаков интоксикации или клинически выраженных отклонений, ухудшения функций органов и систем не выявлено. Во время применения препарата Ипекон® отмечен только один случай нежелательной реакции, имеющей признаки аллергической, без доказательств прямой провокации.
Сокращения
АлАТ — аланинаминотрансфераза, АсАТ — аспартатаминотрансфераза, ВЗК — воспалительное заболевание кишечника, ДВ — действующее вещество, ЖКТ — желудочно-кишечный тракт, ИПК (FIP) — инфекционный перитонит кошек (Feline infectious peritonitis), ИФА — иммуноферментный анализ, МТ — масса тела, ПЭГ — полиэтиленгликоль, ПЦР — полимеразно-цепная реакция, РНК — рибонуклеиновая кислота, ЦНС — центральная нервная система, ЩФ — щелочная фосфатаза, FCoV — Feline Corona Virus (кошачий коронавирус), FECV — Feline Enteric Coronavirus (кишечный коронавирус кошек)
Введение
Инфекционный перитонит кошек (ИПК/FIP, Feline Infectious Peritonitis) — сложное и трудноизлечимое заболевание, вызванное высоковирулентным биотипом широко распространенного кошачьего кишечного коронавируса (FCoV). Последние достижения в области ветеринарии и фармацевтики открыли потенциальные методы лечения ИПК/ FIP. Ингибиторы вирусной протеазы имели революционное значение в таргетной противовирусной терапии. Однако в настоящее время на российском рынке нет ни одного препарата от ИПК/FIP, чья эффективность и безопасность была бы подтверждена должным уровнем проведенных исследований. Препараты, которые вынуждены использовать ветеринарные специалисты, обладают либо контрафактным характером без гарантии качества, либо не прошли полноценные доклинические и клинические исследования. В связи с наличием этических и юридических проблем использования нелицензированных препаратов на российском рынке, возникла острая потребность в безопасном и эффективном препарате для терапии ИПК/FIP, вызываемого FCoV.
Компанией ООО «Ветстем» был разработан двухкомпонентный лиофилизировнный лекарственный препарат под торговым наименованием Ипекон® на основе фармацевтической композиции аналога нуклеозида аденозина — Вефинавира (VS-121354) — ингибитора РНК-зависимой РНК-полимеразы вируса ((2R,3R,4S,5R)-2-(4-аминопирроло[2,1-f][1,2,4] триазин-7-ил)-3,4-дигидрокси-5 (гидроксиметил) оксолан-2-карбонитрила) и таурина (RU2780097C1, RU2791737C1).
Вефинавир (VS-121354) — это низкомолекулярное соединение с прямым противовирусным эффектом в отношении РНК-содержащих вирусов. Является аналогом 1'-цианозамещенного аденина C-нуклеозида рибозы или (2R,3R,4S,5R)-3,4 дигидрокси-5-(гидроксиметил)тетрагидрофуран-2 карбонитрил, замещенный 4-аминопирроло[2,1-f] [1,2,4]триазин-7-ильной группой в положении 2. Это молекулярный предшественник фармакологически активной молекулы нуклеозидтрифосфата для построения вирусной цепи РНК. Механизм действия Вефинавира заключается в остановке репликации вирусной РНК путем ингибирования РНК-зависимой-РНК полимеразы. Это соединение активно изучалось в доклинических исследованиях и показало эффективность в отношении вирусов семейства Coronaviridae и, в частности, в отношении мутированной формы коронавируса кошек (FCoV).
Вторым компонентом препарата Ипекон®, является таурин: он не обладает прямым противовирусным действием, но способен влиять на иммунитет больного животного, благодаря своим антиоксидантным свойствам способен повысить биодоступность Вефинавира (VS-121354) за счет повышения переносимости инъекционной формы. Известно, что таурин — это незаменимая аминокислота для хищников, в частности для кошек. Для поддержания нормальных обменных процессов необходимо постоянное поступление относительно большого количества таурина в организм с кормом. Эта потребность в значительной мере усиливается при наличии воспалительных процессов в ЖКТ, которыми, как правило, сопровождается патогенез ИПК/FIP. Таким образом, таурин, в силу свих метаболических и антиоксидантных свойств, способен усилить терапевтическую эффективность Вефинавира, входящего в состав препарата Ипекон®.
Известно, что механизм действия Вефинавира (VS-121354) реализуется исключительно внутриклеточно, также, как и его аналога, однако они характеризуются низкой биодоступностью и практически не растворимы в воде, что затрудняет получение лекарственных форм на этапе разработки, обеспечивающих достаточно терапевтическую концентрацию вещества в организме. Среди нелицензированных препаратов, эффективность и безопасность которых не может быть адекватно оценена из-за отсутствия централизованных исследований и адекватного сбора данных о клиническом применении, большую часть составляют растворы для инъекций с вариативным содержанием ДВ и более чем одним вспомогательным компонентом, среди которых этанол, пропиленгликоль, ПЭГ и регулирующие pH агенты (до значения pH 1,5…1,8). Данные компоненты позволяют раствору быть стабильным в течение нескольких месяцев, однако некоторые из них также ответственны за нежелательные реакции в местах введения (боль, абсцессы, язвы). Несмотря на жидкую форму композиций и возможность транспортировки и хранения в нормальных условиях, данные об их стабильности и активной концентрации не имеют достаточного подтверждения. Срок годности таких растворов составляет не более 12 мес. Таким образом, во время курса терапии животное вынуждено получать разные варианты раствора. Все это привело к необходимости создания лекарственного препарата с доказанной эффективностью и безопасностью, адекватным профилем стабильности, без наличия токсичных вспомогательных компонентов.
Материалы и методы
Дизайн исследования.
В период с 05 июня 2023 года по 09 февраля 2024 года было проведено официально зарегистрированное мультицентровое рандомизированное клиническое исследование нового препарата «Ипекон®» для лечения ИПК/FIP.
В апреле 2024 года было проведено официально зарегистрированное дополнительное постклиническое исследование (посредством методов ПЦР и ИФА) животных, прошедших курс терапии препаратом Ипекон®, в рамках клинического исследования противовирусной активности к ИПК/FIP.
В клинических и постклинических исследованиях использовали методы прямой и не прямой диагностики.
Места проведения исследования.
Ветеринарная клиника «Триовет» (105094, Россия, г. Москва); ветеринарная клиника «Центр ветеринарной медицины «АВЕТТУРА» (115477, Россия, г. Москва); ветеринарная клиника «Кибела» (129301, Россия, г. Москва).
Животные.
В исследование включили 28 кошек, в возрасте от 6 месяцев до 11 лет. Из них 18 животных с экссудативной и 10 с неэкссудативной («сухой») формой ИПК/FIP.
Критерии включения животных в исследование:
Клинические признаки ИПК/FIP; подтверждение диагноза ИПК/FIP прямыми либо косвенными методами диагностики.
Критерии невключения животных в исследование:
Сопутствующие онкологические процессы; прием прочих ингибиторов FIP в составе лекарственных препаратов в течение последней недели; хронические вирусные заболевания (FIV/FELV), неуточненные заболевания со схожим с ИПК/FIP симптомокомплексом.
Условия содержания животных.
В условиях стационара ветеринарной клиники «Триовет» в течение первых 14 дней лечения находилось двое животных. Температура воздуха в стационаре 18…24 °С, влажность 65…75 %. Кормление 2 раза в день промышленными кормами. Доступ к воде — свободный. Животные в удовлетворительном стабильном состоянии передавались владельцам, содержание — в условиях городских квартир. Кормление в период терапии оставляли без изменений. Доступ к воде — свободный.
Исследуемый препарат.
Ипекон® — истинный противовирусный препарат для лечения ИПК, содержащий два ДВ: Вефинавир (VS-121354) и таурин.
Лекарственная форма:
Лиофилизат для приготовления раствора для инъекций. Препарат Ипекон® представляет собой комплект из флакона с лиофилизатом и флакона с растворителем. В одном флаконе лиофилизата в качестве ДВ содержится: 80 мг Вефинавира (VS-121354) и 180 мг таурина, а также вспомогательные вещества: бетадекса сульфобутилата натрия 2,16 г, хлористоводородной кислоты раствор 10М q.s. (для доведения pH). Один флакон растворителя для Ипекон® содержит воду для инъекций 4 мл. Объем готового раствора препарата после добавления всего объема растворителя к лиофилизату составляет 5 мл.
Организация-разработчик:
ООО «Ветстем» (121205, Россия, г. Москва).
Порядок применения препарата.
Готовый раствор вводили подкожно ежедневно, один раз в день, с интервалом между инъекциями 24 ч в течение всего курса лечения.
Животные были распределены на 3 группы с учетом стартовой разовой дозы препарата Ипекон®: 8 мг/кг, 10, 12 мг/кг (стартовой принята разовая доза, которая назначалась более 10 дней в течение первых двух недель лечения), а также формы ИПК/FIP (экссудативная, не экссудативная, офтальмологическая, неврологическая), тяжести состояния пациента на момент первичного приема (в рамках клинического исследования).
Препарат Ипекон® был назначен:
- в стартовой дозе 8 мг/кг пациентам с экссудативной формой ИПК/FIP;
- в стартовой дозе 10 мг/кг пациентам с экссудативной формой ИПК/FIP в тяжелом состоянии или пациентам с неэкссудативной («сухой») формой (при наличии офтальмологической симптоматики — увеит, ирит, слезотечение, болезненность глаз);
- в стартовой дозе 12 мг/кг пациентам с неэкссудативной («сухой») формой ИПК/FIP, имеющим выраженные неврологические признаки, и пациентам с экссудативной формой в крайне тяжелом состоянии.
В случае слабой динамики терапии допускалось повышение разовой дозы на 2 мг/кг с целью достижения желаемого терапевтического эффекта.
В течение всего периода терапии осуществлялся еженедельный контроль МТ животных.
Оценка эффективности.
Оценка эффективности лечения была комплексной, с учетом данных клинического осмотра, результатов общеклинического и биохимического анализов крови, УЗИ внутренних органов. Мониторинг указанных параметров проводили на первичном (0 день) и повторных приёмах, регламентированных в соответствии с дизайном клинического исследования: по окончании основного курса сочетанной симптоматической терапии (10…14-й день лечения), после первого месяца лечения (30…35-й день), после второго месяца лечения (60…65-й день), по окончании курса препарата Ипекон® (75…90-й день). Оценивали следующие параметры:
- общеклинические показатели: активность и аппетит животных, признаки дегидратации, степень гидратации кожи, цвет видимых слизистых оболочек, температуру тела, частоту актов мочеиспускания и дефекации, признаки одышки и т. д.;
- характерные признаки заболевания ИПК/FIP: асцит, наличие гидроторакса, неврологические симптомы (атаксия, нарушение координации, анизокория, увеит, панофтальмит и т. д.), лимфоаденопатия. При экссудативной форме оценивали объем выпотной жидкости, исследовали ее цитологический состав;
- общеклинические показатели крови: гематокрит, гемоглобин, эритроциты, лейкоциты, тромбоциты, лейкоформула.
- биохимические показатели крови: общий белок, альбумины, глобулины, соотношение альбумин/глобулин, глюкоза, АсАТ, АлАТ, мочевина, креатинин, общий и прямой билирубин.
- УЗИ-симптомы: исследование проводилось мик- роконвексным датчиком с частотой 2,6…13,2 МГц и линейным датчиком с частотой 3,0…14,0 МГц.
- местно-раздражающее действие: наличие припухлости в месте инъекции, ее размеры, признаки болезненности, местной гипертермии, местной воспалительной реакции и т.д.
Животных взвешивали в день начала лечения (до введения препаратов) и регулярно 1 раз в неделю, в том числе на повторных приемах.
В посттерапевтический период проведена оценка:
- терапевтической эффективности препарата Ипекон® (в посттерапевтический период длительностью от 6 до 12 месяцев путем телефонного сбора анамнеза);
- вероятности возникновения рецидивов заболевания ИПК/FIP у животных, прошедших курс терапии препаратом Ипекон® (в связи с отсутствием иных методов постерапевтической диагностики ИПК/ FIP — ИФА сыворотки крови животных с целью определения титра антител FCoV);
- наличия носительства FCoV (в связи с отсутствием иных методов постерапевтической диагностики — ПЦР крови для выявления РНК FCoV).
Статистическая обработка.
Статистический анализ выполнен общепринятыми методами с использованием специальных программ (Prism 7.0). Для проверки нормальности распределения использовали критерий Шапиро-Уилка. При нормальном распределении использованы параметрические методы статистики (t-критерий Стьюдента, парный t-критерий Стьюдента, ANOVA); при распределении, отличном от нормального, использованы методы непараметрической статистики (критерии Манна Уитни, Краскела-Уоллиса, Вилкоксона). Результаты в таблицах представлены как среднее ± стандартная ошибка среднего (Mean ± SEM), если не указано иное. Различия между группами считаются статистически значимыми, если значение р не превысит 0,05.
Результаты
Период от начала заболевания ИПК/FIP до включения пациента в исследование составлял от 3 дней до 3 месяцев; 17 пациентов до включения в исследование лечения не получали, у 11 пациентов предшествующая симптоматическая/паллиативная терапия не обеспечила положительной динамики.
Из 28 животных с диагностированным ИПК/FIP, включенных в исследование, у 4 (14,3 %) пациентов зафиксирован летальный исход, вызванный полиорганной недостаточностью, обусловленной этапом патологического процесса, спровоцированного ИПК/FIP, из них у трех на 3…4-е сутки, у одного — на 7-й день. Остальные 24 кошки (85,7%) на момент окончания курса Ипекон® и завершения исследования имели статус «клиническое выздоровление».
Динамика общего состояния животных.
На первичном приеме у животных отмечали угнетение общего состояния, слабость, дегидратацию, увеличение лимфоузлов брюшной/грудной полостей, гипертермию (более, чем в 90 % случаев), снижение или отсутствие аппетита, потерю МТ (0,3…1,5 кг); примерно у 75 % пациентов проявлялись нарушения работы ЖКТ (у преобладающего большинства копростаз, у меньшей части — диарея). У пациентов с экссудативной формой наблюдали клинические признаки асцита, у одного пациента — увеличение мошонки/орхит (вследствие отека/выпота), затрудненное дыхание (при плевральном выпоте). У животных с «сухой», окулярной и неврологической, неэкссудативной формой было отмечено неспецифическое поведение, нарушение координации, анизокория, шаткость походки, увеит, конъюнктивит, изменения сетчатки, нистагм, иногда судороги.
Согласно результатам УЗИ: увеличение лимфоуз лов брюшной/грудной полостей, селезенки, пиогранулематозные изменения внутренних органов (в первую очередь в лимфоузлах, селезенке, кишечнике, печени, почках), а также признаки диффузных из менений почек, характерных для острого процесса/ нефрита/гломерулонефрита, признаки хронического энтерита/хронической энтеропатии; умеренного острого энтерита, в т. ч. по принципу неспецифического ВЗК, гепатопатии, холангита, панкреатита. У пациентов с экссудативной формой в брюшной или плевральной полости определяли наличие выпотной жидкости.
Согласно показателям крови: лейкоцитоз или, наоборот, у некоторых животных критическая лейкопения (содержание лейкоцитов 2…4×10^9 кл/л), нейтрофилия, лимфоцитопения, эритроцитопения, низкий гематокрит (у преобладающего числа пациентов 12…24 %), тромбоцитопения, а также гипергаммаглобинемия, высокий уровень общего белка, гипоальбунемия, деструктивно отражающаяся на гиперглобулинемии, соотношение alb/glob ниже 0,4 % , повышение содержания билирубина, активности печеночных трансфераз, ЩФ.
В первые семь дней резкая отрицательная динамика с последующей гибелью пациентов наблюдалась в 4-х случаях. Данные животные поступили в клинику в тяжелом состоянии, с признаками обезвожи вания, анорексии и прогрессирующей полиорганной недостаточности. Препарат Ипекон® в соответствии с формой заболевания был назначен 3-м животным в дозе 10 мг/кг (гибель на 3…4-й день лечения) и 12 мг/кг (гибель на 7-й день лечения), данные животные параллельно проходили лечение в условиях интенсивной терапии и реанимации.
У остальных животных после проведенной сочетанной терапии (симптоматическая, инфузионная, патогенетическая) состояние сохранялось стабильным, прослеживалась положительная динамика: животные стали активнее, у них нормализовался аппетит, исчезли признаки дегидратации, видимые слизистые оболочки бледно-розового или розового цвета, температура тела в пределах физиологических границ. Частота дефекации за первые две недели нормализовалась примерно у 90 % животных с первоначальными нарушениями, а к концу первого месяца лечения — у всех. Улучшение общего состояния, нормализация работы ЖКТ сопровождались постепенным набором МТ. У кота с тяжелыми неврологическими симптомами (судороги) на момент включения в исследование (в начале терапии) этот симптом больше не наблюдался.
В течение первого месяца лечения у двух паци ентов группы «10 мг/кг» с экссудативной формой заболевания, несмотря на постепенное улучшение лабораторных показателей, происходило активное накопление выпота, что потребовало частичного его отведения с целью профилактики сдавливания жизненно важных органов и систем и повышения каче ства проводимой терапии. В дальнейшем состояние этих животных улучшилось, объем выпотной жидкости постепенно уменьшался до следового уровня (без принудительного/дополнительного центеза).
По результатам оценки динамики после первых двух-трех недель лечения было принято решение о повышении дозы только у трех пациентов.
На протяжении второго-третьего месяца терапии положительная динамика прослеживалась вплоть до окончания курса препарата Ипекон®. У трех животных несмотря на общее улучшение состояния отмечались признаки отсутствия положительной визуальной динамики: лимфоаденопатии; кратко временные эпизоды спонтанной гипертермии; неразрешающейся, слабо регенеративной анемии; наличия жидкости в брюшной полости, что в период с 35-го по 47-й день не дало ожидаемого терапевтического эффекта и послужило причиной увеличения разовой дозы. Предпринятые действия позволили стабилизировать состояние, купировать нежелательные симптомы и обеспечить положительную динамику. Ни у одного пациента в течение 2-го и 3-го месяца терапии не отмечено рецидивов асцита, а также появления новых (неврологических, офтальмологических) признаков заболевания. У пациентов с «сухой» формой заболевания отмечено отсутствие ранее выявляемой неврологической симптоматики, включая тяжелые неврологические проявления (судороги, атаксия, частичный парез тазовых/грудных конечностей вследствие вовлечения органов ЦНС). У животного с тяжелой офтальмологической формой заболевания наблюдалась оптимальная положительная динамика. При УЗИ отмечена положительная или слабоположительная динамика в отношении размеров лимфоузлов, а также изменений в печени, почках, селезенке.
По завершении курсового лечения препаратом Ипекон® все 24 кошки были активны, имели хороший аппетит, основные физиологические показатели в пределах нормальных значений. Внешних клинических проявлений или прогрессирования вирусного перитонита не выявлено ни у одного животного; по заключению ветеринарных специалистов, все 24 кошки имели статус «клиническое выздоровление».
Динамика массы тела.
У всех животных (за исключением погибших в течение первой недели) проводимая терапия сопровождалась положительной динамикой МТ (рис. 1). Уже после первых двух трех недель терапии у большинства животных МТ увеличилась на 100…200 г. Данный показатель на протяжении всего исследования постепенного возрастал до стабилизации, согласно индивидуальным особенностям пациента (возраст, пол, порода).
Динамика лабораторных показателей анализов крови.
Динамика лабораторных показателей крови пациентов отражена на рис.2.
В первый месяц во всех группах наблюдалась тенденция к нормализации количества лейкоцитов: у пациентов с лейкоцитозом — понижение, у пациентов с лейкопенией — повышение. При этом происходил процесс нормализации уровня нейтрофилов и лимфоцитов: снижение доли нейтрофилов и повышение доли лимфоцитов. Также после первых двух недель терапии содержание эритроцитов, гемоглобина, показатель гематокрита поднялись выше исходных значений. Согласно данным биохимического анализа крови, в результате сочетанной терапии у большинства животных отмечены положительные изменения: нормализация активности печеночных трансфераз, содержания общего и прямого билирубина. Понижение уровня глобулинов отмечалось после первого месяца лечения. Только у части пациентов в первый месяц терапии наблюдалась умеренная отрицательная динамика отдельных показателей: у трех пациентов произошло повышение активности печеночных трансфераз (преимущественно АлАТ), а у одного пациента — ЩФ; у четырех пациентов — усиление гиперглобулинемии и заметное увеличение содержания общего белка; повышение содержания мочевины у 5 пациентов.
Отмеченная положительная динамика сохранилась и в последующие периоды наблюдения. Во всех группах отмечено постепенное увеличение содержания эритроцитов, тромбоцитов, гемоглобина и рост гематокрита. Содержание лейкоцитов — в пределах нормы у всех животных за исключением трех пациентов. При этом сохранялась положительная динамика в количестве нейтрофилов и лимфоцитов. Содержание нейтрофилов ниже, чем исходное, а лимфоцитов, наоборот, выше, чем исходное на 10…30 %. Усредненные значения данных показателей (доля нейтрофилов и лимфоцитов) после окончания 1-го и 2-го месяца терапии препара том Ипекон®, а также в конце периода наблюдений находились в пределах референсных значений. Только у трех животных (по одному из каждой группы) по окончании курсового лечения доля нейтрофилов превышала 80 %, доля лимфоцитов была не более 15 % при содержании лейкоцитов 7,3…10,7 тыс/мкл. Во всех группах следует отметить увеличение доли эозинофилов на протяжении всего периода наблюдений, все отмеченные изменения доли эозинофилов происходили в пределах референсных значений.
Во второй и третий месяц терапии большинство биохимических показателей находилось в пределах референсных значений либо незначительно их превышало. По всем показателям, исходно отклонявшимся от нормы, прослеживалась положительная динамика. Содержание глобулинов — ниже исходных значений во всех группах на уровне отчетливой тенденции, что обеспечило соотношение альбуминов к глобулинам на уровне 0,6…0,75. Можно отметить единичные случаи повышенной активности АлАТ, ЩФ.
По завершении курса препарата Ипекон® у превалирующего большинства пациентов (22 кошки) все контролируемые биохимические показатели были в пределах референсных значений или у некоторых животных (7 из 22 кошек) общий белок и/или глобулины немного превышали верхнюю границу нормы.
Следует отметить, что у 13-ти из 24-х пациентов за время лечения уровень мочевины и креатинина заметно повысился (в некоторых случаях более, чем в 2 раза относительно исходных значений), но на момент финального осмотра находился в пределах референсных значений у всех животных за исключением одного пациента, поступившего с тяжелой неврологической формой ИПК/FIP.
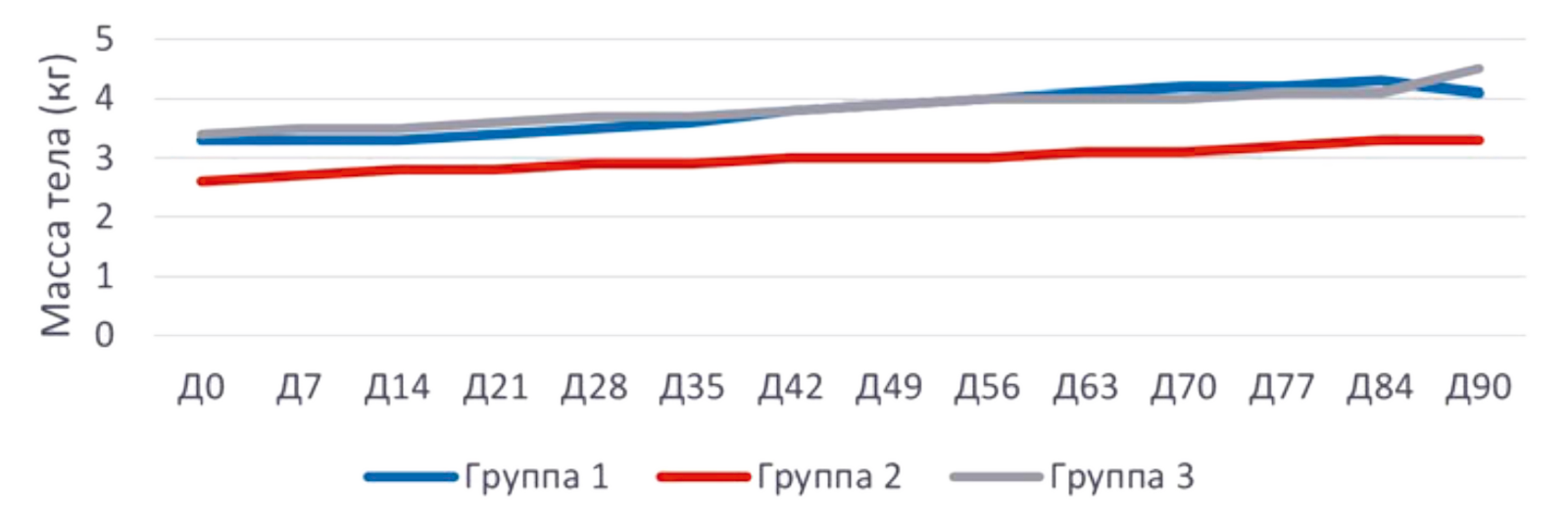
Рис. 1. Динамика массы тела (в кг) кошек с диагнозом ИПК/FIP при терапии препаратом «Ипекон®»
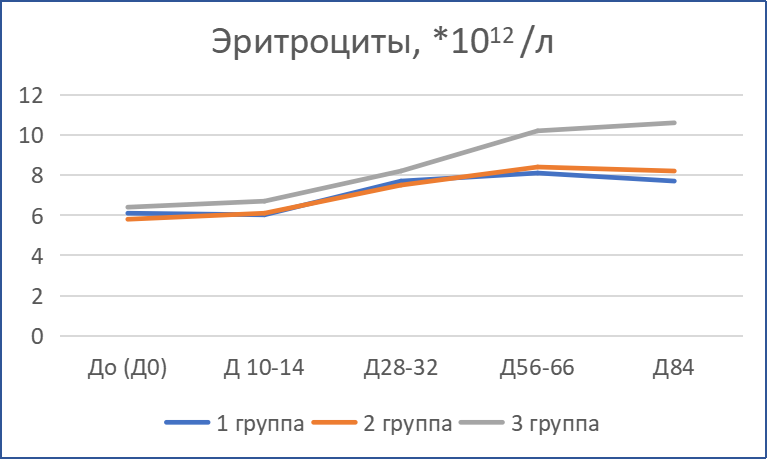
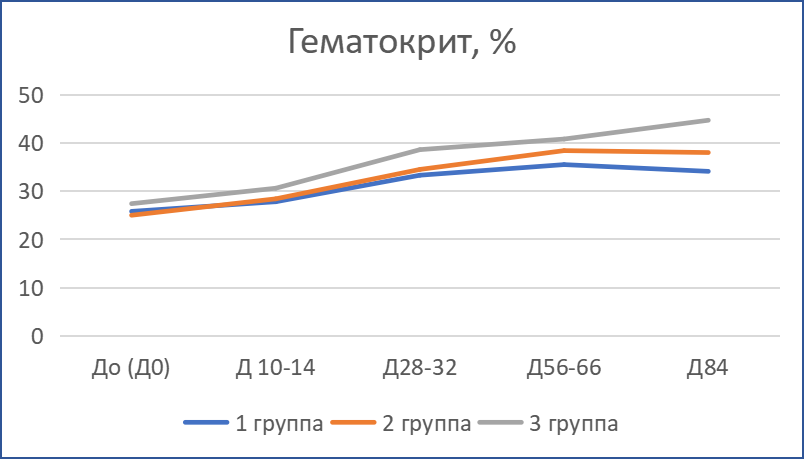
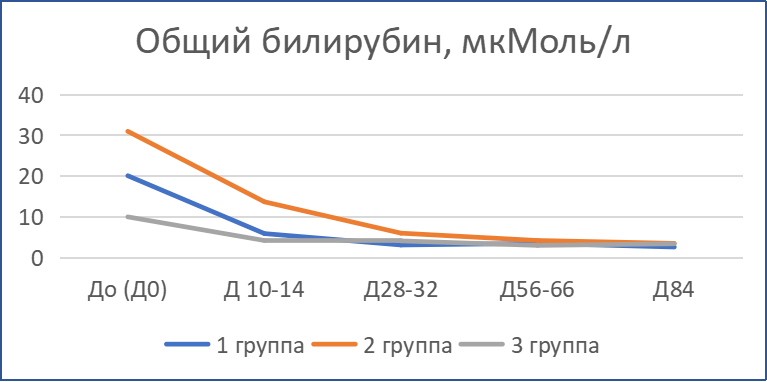
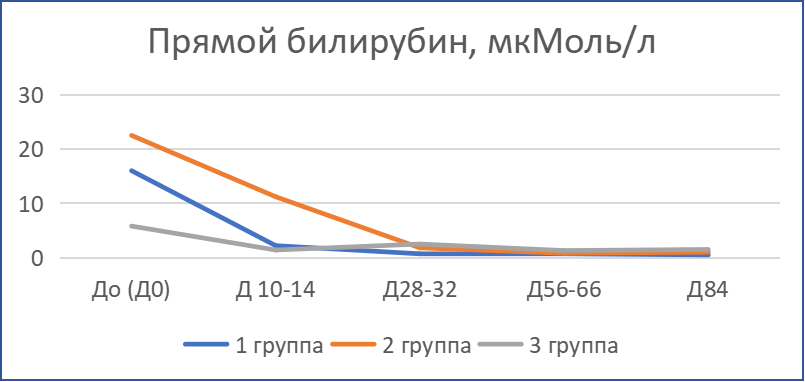
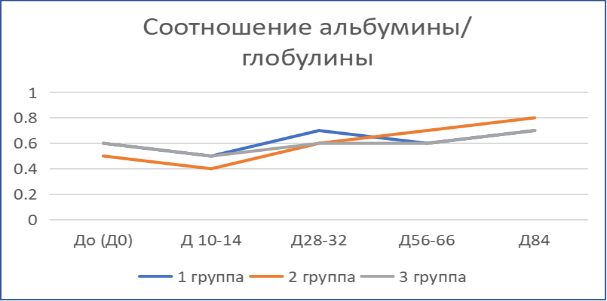
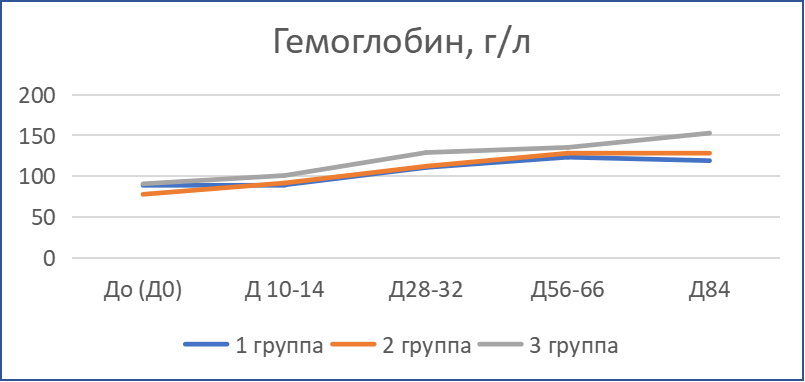
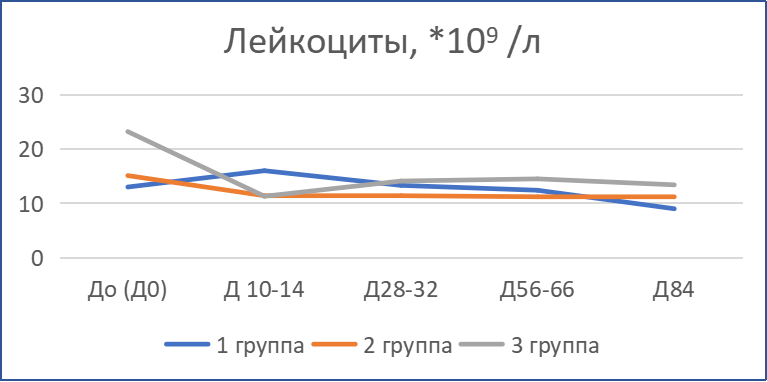
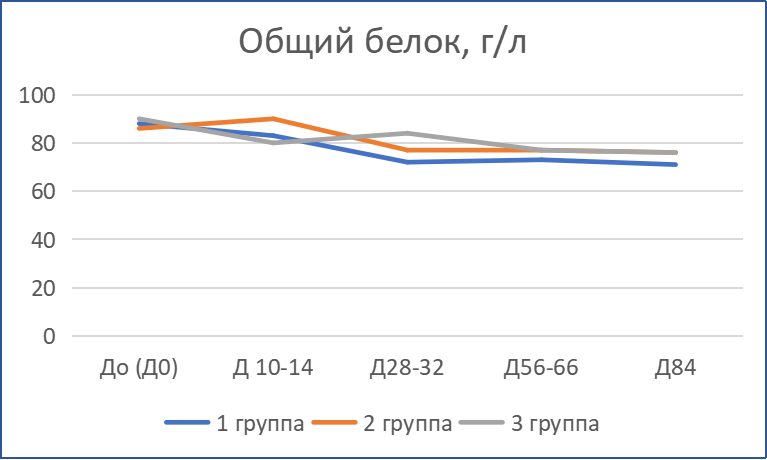
Рис. 2. Динамика лабораторных показателей анализов крови кошек с диагнозом ИПК/FIP при терапии препаратом «Ипекон®»
Нежелательные явления, побочные эффекты.
При введении препарата все животные испытывали дискомфорт, а некоторые и боль, однако проявляли индивидуальную чувствительность по-разному: некоторые «стойко» переносили инъекции, а другие сопровождали процедуру введения агрессивным поведением.
При курсовом применении препарата Ипекон® (84 дня) у 3 животных (10,7 %) в местах введения препарата наблюдалась индивидуальная реакция в виде локального уплотнения подкожно-жировой клетчатки, с признаками воспаления. Участки гиперчувствительности зажили самостоятельно без вспомогательного лекарственного воздействия. У одного пациента предположительно отмечались признаки аллергической реакции на фоне применения препарата Ипекон®. Данное явление разрешилось самостоятельно без дополнительной фармакотерапии в течение 2…5 дней (выбирали альтернативные точки введения препарата). Непосредственная провокация аллергического процесса препаратом Ипекон® не доказана, тем не менее процесс был зафиксирован. Других нежелательных реакций отмечено не было.
Вероятность возникновения рецидивов.
По результатам телефонного сбора анамнеза все животные (24 кошки), прошедшие противовирусную терапию препаратом Ипекон®, ведут активный образ жизни и не имеют клинических симптомов ИПК/FIP. Из них 16 животных приняли участие в постклиническом исследовании и прошли диагностику методами ПЦР и ИФА, остальные 8 животных не смогли пройти обследование по личным обстоятельствам владельцев.
У 100 % животных, прошедших диагностическое обследование ПЦР на выявление возбудителя ИПК/FIP — РНК FCoV, получен отрицательный результат, интерпретирующий отсутствие виремии на момент диагностики.
Иммуноферментный анализ сыворотки крови на определение титра антител класса IgG к FCoV продемонстрировал результаты, представленные в таблице 2. При этом 81,25 % кошек имеют титр антител 1:3200 (расшифровка: 1:3200 и выше — диагностический титр ИПК/FIP); 12,5 % кошек имеют титр антител 1:1600 (расшифровка: 1:800…1:1600 — животное болеет коронавирусным гастроэнтеритом, с высокой вероятностью выделения вируса во внешнюю среду); 6,25 % кошек имеют титр антител 1:800 (см. предыдущую расшифровку). Таким образом 81,25 % животных, прошедших диагностику методом ИФА, имеют титр антител к FCoV в диагностическом пределе. При этом 18,75 % животных обладают титром антител к FCoV, который свидетельствует с высокой долей вероятности о выделении вируса во внешнюю среду. Данный метод диагностики не информативен в отношении установления диагноза ИПК/FIP без особых клинических проявлений, в нашем случае он статистически значим в постклиническом исследовании.
Обсуждение
Проведенное клиническое исследование показало, что применение препарата Ипекон® при лечении вирусного перитонита кошек обеспечивает выраженный терапевтический эффект — клиническое выздоровление зарегистрировано у 85,7 % пациентов (24 кошки из 28). Результаты терапии вирусного перитонита кошек препаратом Ипекон® демонстрируют его несомненные противовирусные свойства и высокую терапевтическую эффективность, которая в случае своевременной диагностики и начала терапии способна достигать 100 %. По окончании курсового применения препарата Ипекон® состояние животных было стабильным, рецидивов заболевания или значимого ухудшения функций жизненно важных органов и систем не отмечалось.
Выбранный режим дозирования позволил достичь выраженного терапевтического эффекта у девятнадцати пациентов без коррекции дозы. У пяти пациентов проведена коррекция дозы в связи с недостаточной динамикой в первый месяц терапии. Повышение дозы на 2 мг/кг хорошо переносилось животными и обеспечивало устранение нежелательных симптомов и положительные последствия терапевтической стратегии.
Также во всех группах при курсовом применении препарата Ипекон® наблюдался постепенный рост количества эозинофилов (в пределах референсных значений), мочевины и креатинина (в пределах референсных значений за исключением одного пациента). При этом клинических симптомов нарушения функции мочевыделительной системы или проявления других нежелательных симптомов не отмечено.
В процессе применения препарата Ипекон® отмечен один случай нежелательной реакции, имеющей признаки аллергической, без наличия доказательной базы прямой провокации процесса.
В результате постклинического исследования эффективности у 100 % включенных в исследование животных был получен отрицательный результат ПЦР на выявление возбудителя заболевания — РНК FCoV в биоптате, что на фоне отсутствия клинических симптомов, свойственных ИПК/FIP, говорит об отсутствии в свободной субстанции — крови — вирусных частиц, клинической/субклинической вирусной виремии. При этом необходимо отметить, что несмотря на то, что ПЦР является высокоточным методом выявления инфекционного агента, нельзя исключать, что концентрация возбудителя в исследуемой пробе может оказаться ниже, чем порог чувствительности аппарата. Но 100%-й отрицательный результат на фоне клинического здоровья всех животных с отсутствием патологической симптоматики, подозрительной в отношении ИПК/FIP, с высокой долей вероятности исключают такую возможность.
По результатам проведенного ИФА сыворотки крови 81,25 % кошек имеют титр антител класса IgG выше диагностического титра ИПК/FIP (1:3200). 18,75 % животных обладают титром антител к FCoV, который свидетельствует с высокой долей вероятности о выделение вируса во внешнюю среду (1:1600…1:800). Наличие таких данных ИФА на фоне отрицательных результатов ПЦР при системном выявлении коронавирусной инфекция кошек и полном клиническом здоровье животных, свободных от признаков ИПК/FIP, как клинически, так и в анамнезе посттерапевтического периода могут свидетельствовать о реакции организма достаточно высоким титром антител на местное развитие патологического процесса, вызванного FECV, а высокий титр антител направлен на его нейтрализацию. При этом наличие иммунной реакции на FECV может объясняться его высокой вирулентностью и вероятным наличием контакта (с возможностью реинфицирования) животных, участвующих в постклиническом исследовании.
Заключение
Основное лечение ИПК/FIP заключается в использовании противовирусной терапии с доказанной эффективностью. Только лечение истинно противовирусными препаратами обеспечит полное выздоровление.
Проведенные клинические исследования препарата Ипекон® продемонстрировали его выраженную терапевтическую эффективность при лечении ИПК/ FIPV: 85,7 % пациентов по окончании курсового лечения имели статус «клиническое выздоровление». Установлена хорошая переносимость препарата Ипекон® при многократном подкожном применении. Несмотря на отмеченный дискомфорт, испытываемый пациентом при введении препарата, признаков интоксикации или клинически выраженных отклонений, ухудшения функций органов и систем выявлено не было. Во время применения препарата Ипекон® отмечен только один случай нежелательной реакции, имеющей признаки аллергической, без доказательств прямой провокации.
Курсовое применение препарата Ипекон® кошкам с различной формой вирусного перитонита обеспечивает быструю стабилизацию состояния пациента, положительную динамику и ослабление/устранение основных симптомов заболевания уже в течение первого месяца лечения. Соблюдение рекомендованного режима дозирования (ежедневно 1 раз в сутки в течение 84 дней в разовых дозах в соответствии с проектом инструкции) обеспечивает минимальную летальность и высокую выживаемость пациентов с достижением статуса «клиническое выздоровление» по завершении курсового лечения без рецидивирующих последствий в течение 6…12 месяцев наблюдений.
Препарат Ипекон® рекомендован к включению в схему лечения вирусного перитонита кошек в качестве ключевого противовирусного лекарственного средства.
Конфликт интересов
О конфликте интересов не сообщается.
Библиография
- Addie, D. Feline infectious peritonitis. ABCD guidelines on prevention and management / D. Addie, S. Belák, C. Boucraut-Baralon, H. Egberink, T. Frymus, T. Gruffydd-Jones, K. Hartmann, M.J. Hosie, A. Lloret, H. Lutz, F. Marsilio, M.G. Pennisi, A.D. Radford, E. Thiry, U. Truyen, M.C. Horzinek // J Feline Med Surg. — 2009 Jul. — No. 11(7). — pp. 594-604. doi: 10.1016/j. jfms.2009.05.008. PMID: 19481039; PMCID: PMC7129471.
- Dickinson, P.J. Antiviral treatment using the adenosine nucleoside analogue GS 441524 in cats with clinically diagnosed neurological feline infectious peritonitis / P.J. Dickinson, M. Bannasch, S.M. Thomasy, V.D. Murthy, K.M. Vernau, M. Liepnieks, E. Montgomery, K.E. Knickelbein, B. Murphy, N.C. Pedersen // J Vet Intern Med. — 2020 Jul. — No. 34(4). — pp. 1587-1593. doi: 10.1111/ jvim.15780. Epub 2020 May 22. PMID: 32441826; PMCID: PMC7379040.
- Meli, M.L. Fecal Feline Coronavirus RNA Shedding and Spike Gene Mutations in Cats with Feline Infectious Peritonitis Treated with GS-441524 / M.L. Meli, A.M. Spiri, K. Zwicklbauer, D. Krentz, S. Felten, M. Bergmann, R. Dorsch, K. Matiasek, M. Alberer, L. Kolberg, U. von Both, K. Hartmann, R. Hofmann Lehmann // Viruses. — 2022 May. — Vol. 17. — No. 14(5). — pp. 1069. doi: 10.3390/v14051069. PMID: 35632813; PMCID: PMC9147249.
- Pedersen, N.C. Virologic and immunologic aspects of feline infectious peritonitis virus infection / N.C. Pedersen. — Adv Exp Med Biol. — 1987. — No. 218. — pp. 529-550. doi: 10.1007/978-1-4684-1280-2_69. PMID: 2829567.
- Sykes, J.E. Greene's Infectious Diseases of the Dog and Cat / J.E. Sykes. — Book Fifth Edition, Elsevier Inc. 2023. doi: 10.1016/C2014-0-03934-2 ISBN 978-0-323-50934-3.
- Tasker, S. Feline Infectious Peritonitis: European Advisory Board on Cat Diseases Guidelines / S. Tasker, D.D. Addie, H. Egberink, R. Hofmann-Lehmann, M.J. Hosie, U. Truyen, S. Belák, C. Boucraut-Baralon, T. Frymus, A. Lloret, F. Marsilio, M.G. Pennisi, E. Thiry, K. Möstl, K. Hartmann // Viruses. — 2023 Aug. — Vol. 31. — No. 15(9). — pp. 1847. doi: 10.3390/v15091847. PMID: 37766254; PMCID: PMC10535984.
- Thayer, V. 2022 AAFP/EveryCat Feline Infectious Peritonitis Diagnosis Guidelines / V. Thayer, S. Gogolski, S. Felten, K. Hartmann, M. Kennedy, G.A. Olah // J Feline Med Surg. — 2022 Sep. — No. 24(9). — pp. 905-933. doi: 10.1177/1098612X221118761. Erratum in: J Feline Med Surg. 2022 Dec;24(12): e676. doi: 10.1177/1098612X221126448. PMID: 36002137; PMCID: PMC10812230.
- Викторова, Е.В. Композиция для лечения инфекционного перитонита кошек / Викторова Е.В., Колесников Н.В., Решетнев А.В., Плющий И.В., Вирясова Н.А. — Патент. 2021. RU2780097C1.
- Викторова, Е.В. Лиофилизированная композиция ингибитора РНК по лимеразы для лечения инфекционного перитонита кошек, вызываемого кошачьим коронавирусом / Е.В. Викторова, Н.В. Колесников, А.В. Решет нев, Е.И. Короткевич. — Патент. 2023. RU2791737C1.
- Лобанов, П.С. FIP — не приговор: диагностика и терапия инфекционного перитонита кошек / П.С. Лобанов, Л.В. Клетикова, Е.В. Викторова. — Москва - Иваново: Научная библиотека, 2023. — 80 с.
- Михайловская, П.А. Новый подход в лечении вирусного перитонита кошек / П.А. Михайловская, К.М. Кондрашкина, Е.И. Симонова, Е.О. Рысцо- ва // Бюллетень науки и практики. — 2019. — Т. 5. — №5. — С. 210-220.
Контакты
-
ООО «ВЕТСТЕМ»
Резидент инновационного центра «Сколково», ведущий российский разработчик и производитель инновационных ветеринарных препаратов.
vetstem.ru -
Время работы
Пн-Пт: 9:00-18:00
Напишите нам
Заполните форму, и наши специалисты свяжутся с вами в ближайшее время
Где купить Ипекон®
- Препарат доступен на популярных маркетплейсах
-
Wildberries
Перейти в магазин -
Ozon
Перейти в магазин -
Яндекс.Маркет
Перейти в магазин - Имеются противопоказания.
Необходимо проконсультироваться со специалистом